Introducción
La psoriasis es una enfermedad inflamatoria crónica inmunomediada que afecta a alrededor de 60 millones de personas en todo el mundo. Si bien la psoriasis en placas es el subtipo clínico más común, además de ella existen las psoriasis guttata, flexural, pustulosa y eritrodérmica. Además del marcado daño en la piel, tienen un impacto importante con comorbilidad sistémica tanto en forma de artritis psoriásica como de enfermedades cardiacas y metabólicas, y trastornos psicológicos. En 2014, la Organización Mundial de la Salud reconoció la gravedad de la psoriasis como enfermedad no transmisible. Las causas son un diagnóstico tardío, tratamientos insuficientes y estigma social1–3.
La prevalencia de la psoriasis varía considerablemente entre países, desde el 0.05% en Taiwán hasta el 1.88% en Australia. En el Reino Unido, afecta al 1.52% de la población general; no obstante, es más frecuente en áreas de altos ingresos y entre poblaciones envejecidas. Se ha documentado que la afección tiene un patrón bimodal de inicio con picos a los 30-39 años y los 60-69 años en los hombres, y una década antes en las mujeres. Estas tendencias epidemiológicas subyacen a la interacción de factores genéticos y ambientales que contribuyen a su desarrollo4–6.
La etiología de la psoriasis es multifactorial, pero tiene una fuerte predisposición genética. Los estudios más recientes han logrado identificar más de 60 loci que confieren susceptibilidad; el eje IL-23/Th17 es el mecanismo más conocido como uno de los principales impulsores de la proliferación de queratinocitos y la inflamación crónica. Además, subyace la activación desregulada de células T y dendríticas, lo que favorece la producción de diferentes citocinas inflamatorias, tales como las interleucinas (IL) 7 y 22, y el factor de necrosis tumoral alfa (TNF-α). Adicionalmente, factores como la obesidad, el estrés, el tabaco y ciertos fármacos pueden exacerbar la enfermedad, y su morbilidad subraya su naturaleza multifacética y compleja7–12.
Las mejoras en la comprensión de la patogenia de la psoriasis han abierto la puerta al desarrollo de tratamientos altamente específicos y eficaces, transformando la dinámica terapéutica de la afección. Estas opciones incluyen agentes tópicos, fototerapia, tratamientos sistémicos convencionales como metotrexato y ciclosporina, así como terapias biológicas contra el TNF, la IL-17 y la IL-23. No solo han mejorado los resultados clínicos, sino que también han aliviado las cargas sistémicas asociadas con la psoriasis, subrayando la necesidad de un enfoque personalizado y multidisciplinario para las personas con psoriasis13–16.
Método
Se llevó a cabo una revisión narrativa con el objetivo de explorar y sintetizar información relevante sobre los avances terapéuticos en la psoriasis. Para ello, se realizó una búsqueda exhaustiva en las bases de datos Medline, PubMed, EMBASE, Cochrane Library, OVID y ClinicalKey, de artículos publicados en inglés y español. No se estableció un límite temporal en los años de publicación, permitiendo la inclusión de investigaciones tanto recientes como históricas que aportaran valor a la comprensión del tema.
La búsqueda se diseñó utilizando términos MeSH específicos: “[(Psoriasis) OR (Palmoplantaris Pustulosis)] AND (Therapeutics)”. Los criterios de inclusión consideraron artículos originales, revisiones sistemáticas, estudios de práctica clínica real y ensayos clínicos que abordaran la eficacia, la seguridad y los avances terapéuticos en la psoriasis, incluyendo terapias biológicas, tópicas y sistémicas. También se consideraron estudios que discutieran los mecanismos fisiopatológicos subyacentes, comparaciones entre tratamientos y perspectivas futuras en el manejo de la enfermedad. Por otro lado, se excluyeron los artículos duplicados y aquellos que no estuvieran directamente relacionados con el tema central de la revisión. Lo anterior, permitió integrar y analizar críticamente la evidencia disponible, destacando las fortalezas, las limitaciones y las brechas de conocimiento en los tratamientos actuales, e identificando áreas prioritarias para investigaciones futuras en psoriasis.
Resultados
Bimekizumab
El bimekizumab, un inhibidor dual de la IL-17A y la IL-17F, ha tenido resultados promisorios en ensayos clínicos con pacientes con psoriasis entre moderada y grave. En el ensayo de fase IIb BE ABLE, el 79.1% de los pacientes en tratamiento con bimekizumab 320 mg lograron un 90% de mejoría según el Psoriasis Area Severity Index (PASI90) en la semana 12, mientras que el grupo que recibió placebo no mostró ninguna mejoría. Los resultados obtenidos se repiten en los distintos ensayos de fase III. Por ejemplo, el ensayo BE READY coincide con un 91% de PASI90 en el grupo de tratamiento y un 1% en el grupo de placebo en la semana 16, mientras que en el ensayo BE VIVID el 85% del grupo con bimekizumab lograron PASI90, frente al 50% del grupo tratado con ustekinumab y el 15% del grupo con placebo17–19.
El bimekizumab se comparó directamente con el secukinumab, un inhibidor selectivo de la IL-17A, en el ensayo de fase IIIb BE RADIANT. Los resultados mostraron que con bimekizumab el 61.7% de los participantes alcanzaron PASI100 en la semana 16, y el 67% alcanzó el mismo nivel en la semana 48. Comparativamente, en el grupo de secukinumab el 48.9% de los pacientes lograron PASI100 en la semana 16, y solo el 56.2% en la semana 48. La mayor eficacia del bimekizumab en comparación con el secukinumab sugiere su capacidad inhibidora de la IL-17F, que conjuntamente con la IL-17A demostró ser más efectiva que los inhibidores solo de la IL-1719.
El perfil de seguridad del bimekizumab fue manejable en los ensayos clínicos. Los eventos más comunes fueron nasofaringitis, infección del tracto respiratorio superior y artralgias leves. En el ensayo BE RADIANT, la incidencia de candidiasis mucocutánea fue mayor en el grupo de bimekizumab que en el grupo de secukinumab (19.3% frente a 3%). A pesar de ser fácilmente tratable, este efecto secundario respalda la conclusión de que los pacientes deben ser monitorizados en busca de infecciones fúngicas durante el tratamiento con bimekizumab18,19. Este fármaco es una terapia de reemplazo biológica novedosa y efectiva para pacientes con psoriasis moderada a grave, de especial interés en los pacientes no respondedores o con tolerancia a otros biológicos. La inhibición dual de IL-17A y IL-17F ofrece una doble ventaja que produce una mejor tasa de la respuesta clínica como PASI90 y PASI100. A pesar de que se necesitan investigaciones más prolongadas para determinar su efectividad en entornos clínicos, los datos actuales son consistentes con su función como un recurso esencial para el tratamiento de esta enfermedad crónica17,19.
Roflumilast
El roflumilast es un inhibidor altamente potente de la fosfodiesterasa 4, que en un principio fue desarrollado con el propósito de minimizar las exacerbaciones de la enfermedad pulmonar obstructiva crónica. Su acción terapéutica consiste en actuar como un inhibidor de la fosfodiesterasa 4 específico con el objetivo de evitar la degradación del monofosfato de adenosina cíclico (cAMP), generando como consecuencia efectos antiinflamatorios y modulación inmunitaria en distintos tejidos. En el tratamiento de la psoriasis, se ha comprobado que la formulación al 0.3% de roflumilast es segura y efectiva, reduciendo su exposición sistémica y enfocándola a la piel20,21.
En el estudio de máxima exposición farmacocinética y seguridad, se administró roflumilast en crema al 0.3% a 26 pacientes con psoriasis (6 adolescentes y 20 adultos). En 15 días de tratamiento, la biodisponibilidad sistémica fue mínima, de solo el 1.5%, en comparación con el 79% observado con la administración de roflumilast oral. Las concentraciones máximas en plasma fueron de 3.72 ng/ml en los adultos y 1.27 ng/ml en los adolescentes, con un tiempo promedio para la concentración máxima de aproximadamente 11 horas. Estos valores fueron consistentes y estadísticamente constantes22,23.
En los estudios de fase III DERMIS-1 y DERMIS-2, realizados en adultos, adolescentes y niños, la aplicación tópica de roflumilast mostró una exposición sistémica uniforme. A la semana 8 de tratamiento, las concentraciones mínimas previas a la siguiente dosis fueron 1.78 ng/ml para roflumilast y 9.86 ng/ml para su metabolito N-óxido en adultos. Lo anterior permite pensar y considerar la baja absorción sistémica y una farmacocinética favorable para su uso tópico21. En cuanto a la seguridad, se reportaron eventos adversos emergentes en el 30.8% de los pacientes. Los más comunes fueron náuseas (11.5%), molestias auriculares, parestesia en el sitio de aplicación y dolor lumbar, todos de gravedad leve a moderada. Ningún participante interrumpió el tratamiento debido a efectos adversos, y los adolescentes no reportaron ningún evento adverso emergente. Además, las evaluaciones clínicas, como el electrocardiograma, el peso corporal y las escalas de salud mental, no evidenciaron efectos negativos del tratamiento21.
Los resultados de los análisis de concentraciones de roflumilast en la piel indican, en primer lugar, unos niveles mucho mayores en el tejido cutáneo frente al plasma, con una proporción de hasta 126 veces más en el tejido cutáneo. Los resultados sugieren la eficacia localizada del fármaco y la poca conversión a su metabolito activo N-óxido, que limita los efectos sistémicos24,25. En conjunto, estos resultados demuestran que la crema de roflumilast al 0.3% es segura, bien tolerada y eficaz en el tratamiento de la psoriasis. Su perfil farmacocinético único, caracterizado por una baja absorción sistémica y una alta retención cutánea, minimiza el riesgo de eventos adversos sistémicos como los observados con su formulación oral, y optimiza la respuesta terapéutica en las lesiones cutáneas20–22,25.
Apremilast
El apremilast es un inhibidor selectivo de la fosfodiesterasa 4, cuya acción intracelular incrementa los niveles de cAMP, modulando las respuestas inmunitarias innatas y adaptativas. Este mecanismo promueve señales antiinflamatorias regulando citocinas como el TNF-α, la IL-17 y la IL-10, mientras disminuye la actividad citotóxica de las células T CD8+ y las respuestas Th1 y Th17. Su impacto en la función de las células dendríticas, los monocitos y los queratinocitos es clave para mitigar la inflamación crónica observada en la psoriasis26,27.
Tras su administración, el apremilast alcanza su concentración máxima en plasma a las 2-6 horas, con una biodisponibilidad del 73%. Tiene una vida media de 8.2 horas y se metaboliza por múltiples vías, incluyendo el citocromo P450 (CYP). Su eliminación es principalmente renal (el 3% sin cambios). No se identificaron interacciones farmacológicas significativas con inhibidores de CYP como el metotrexato y los anticonceptivos orales, pero los inductores fuertes como la rifampicina reducen su eficacia28,29. En los estudios de fase III ESTEEM 1 y 2, el apremilast (30 mg dos veces al día) logró una reducción significativa PASI-75 en el 33.1% y el 28.8% de los pacientes al alcanzar la semana 16, frente al 5.3% y el 5.8% en los grupos que recibieron placebo (p < 0.0001). Estos efectos se mantuvieron hasta la semana 52, con una respuesta mantenida en el 47-61% de los pacientes. Su eficacia fue particularmente notable en psoriasis de localización específica (ungueal, del cuero cabelludo y palmoplantar) y en reducción del prurito30,31.
Los estudios observacionales sugieren que los pacientes tratados con apremilast tienen menos gravedad inicial (PASI promedio 10-11) que los incluidos en los ensayos clínicos (PASI ~19). La respuesta PASI-75 en series reales varía del 18.8% al 59.3%, con mayores tasas en pacientes con PASI basal bajo. La supervivencia al fármaco a 1 año varió entre el 46.8% y el 75%, siendo el abandono del tratamiento principalmente por eventos adversos o pérdida de eficacia32,33.
El apremilast mostró un perfil de seguridad aceptable. Los eventos adversos más frecuentes fueron diarrea (17.3%), náuseas (15.7%), infecciones respiratorias (15.5%) y cefalea tensional (9.0%). La pérdida de peso (> 5%) ocurrió en un 20% de los pacientes, sin consecuencias clínicas graves. La depresión fue reportada en el 1.4-1.8% de los pacientes, sin aumento de la incidencia con la exposición prolongada. Los eventos cardiovasculares mayores y las infecciones graves tuvieron incidencias comparables a las de la población general31,33.
Tapinarof
El tapinarof es un innovador modulador del receptor de hidrocarburos arílicos (AhR) y representa un avance significativo en la terapia tópica para la psoriasis. Este receptor es un factor de transcripción dependiente de ligando que regula múltiples genes implicados en la homeostasis de la piel, la función de la barrera cutánea y la modulación del estrés oxidativo. En los pacientes con psoriasis, el AhR desempeña un papel clave en la reducción de citocinas proinflamatorias como IL-17 e IL-22, que son fundamentales en la patogénesis de la enfermedad. Además, la activación selectiva de AhR por el tapinarof incrementa la expresión de proteínas como la filagrina y la loricrina, esenciales para la integridad de la barrera cutánea. Este mecanismo también induce respuestas antioxidantes a través de la vía Nrf2, disminuyendo las especies reactivas de oxígeno que contribuyen al daño celular. Así, el tapinarof no solo aborda los aspectos inflamatorios, sino también las alteraciones estructurales y funcionales características de la psoriasis34–36.
En ensayos clínicos de fase IIb y III, el tapinarof ha demostrado una eficacia notable en pacientes con psoriasis en placas de leve a grave. Los estudios han reportado que el uso de tapinarof en crema al 1% una vez al día durante 12 semanas resultó en una mejora significativa del índice PASI-75 en un 56% de los pacientes, mientras que un 40% alcanzaron PASI-90. Estas mejoras fueron evidentes desde las primeras 2 semanas de tratamiento y se mantuvieron hasta 4 semanas después de su interrupción, lo que resalta la durabilidad del efecto terapéutico. En comparación con los vehículos, el tapinarof también mostró beneficios significativos en la reducción de la gravedad de las lesiones y del prurito, con un perfil de seguridad favorable. Los efectos adversos más comunes fueron leves o moderados, como dermatitis de contacto y foliculitis, sin restricciones anticipadas para el uso prolongado37–39.
En el contexto de las terapias tópicas, el tapinarof ofrece ventajas significativas frente a las opciones convencionales, como los corticosteroides y los análogos de la vitamina D, que presentan limitaciones en su duración de uso y riesgos de eventos adversos. Su perfil único de acción, basado en la modulación selectiva del AhR, lo posiciona como un tratamiento alternativo bien tolerado y efectivo. Además, los estudios preclínicos sugieren que su mecanismo de acción tiene potencial para ser aplicado en otras enfermedades inflamatorias de la piel, como la dermatitis atópica. El avance hacia ensayos clínicos de fase III proporciona una base sólida para ampliar el uso clínico de tapinarof, mejorando tanto la calidad de vida como los desenlaces clínicos en los pacientes con psoriasis40–42.
Perspectivas futuras
El aumento en la comprensión de la fisiopatología de la psoriasis y el desarrollo de agentes nuevos, tales como el bimekizumab, el roflumilast, el apremilast y el tapinarof, han transformado el panorama terapéutico y ofrecen oportunidades adicionales para el manejo individualizado de la enfermedad crónica. Con su combinación de acción dual sobre la IL-17A y la IL-17F, el bimekizumab ha demostrado porcentajes sobresalientes de PASI90 y PASI100, mientras que el roflumilast ofrece un perfil de seguridad y eficacia en fórmula tópica con casi nula exposición sistémica. Por otro lado, el uso en localizaciones particulares y en casos de tolerancia mantiene la expansión del apremilast, mientras que el tapinarof redefine los tratamientos tópicos al combinar propiedades antiinflamatorias, antioxidantes y restauradoras de la barrera cutánea mediante una modulación selectiva del AhR. Los futuros desarrollos requieren estudios a largo plazo sobre la seguridad y la eficacia en diversas poblaciones, estudios comparativos y estudios secundarios de combinaciones terapéuticas guiadas por mecanismos de acción compatibles o totalmente diferentes. Estas estrategias podrían potenciar el impacto clínico e impulsar cambios significativos en la calidad de vida de los pacientes, lo que destaca la importancia de enfoques multidisciplinarios y personalizados a considerar por cualquier médico dentro de la atención de esta condición (Fig. 1).
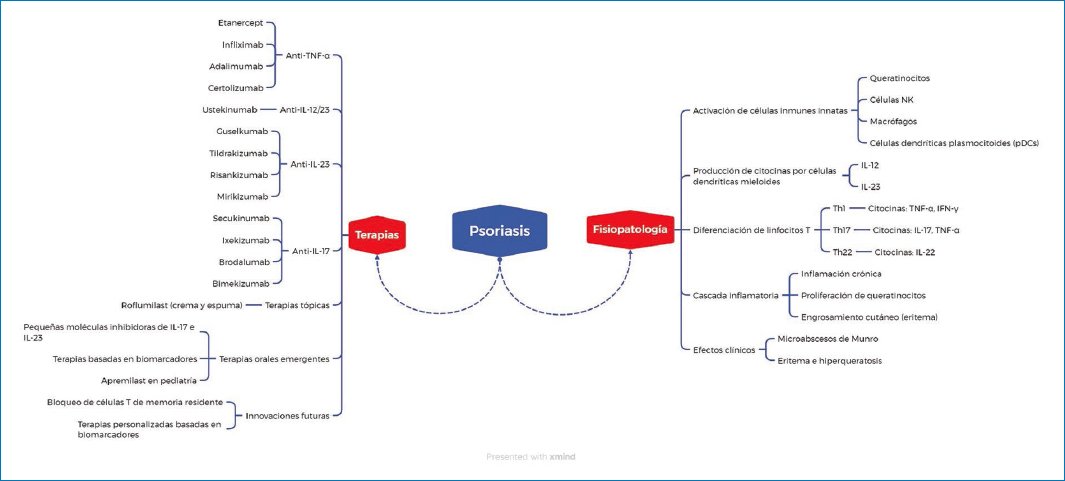
Figura 1. Principales aspectos fisiopatológicos y terapéuticos de la psoriasis.
Conclusión
La psoriasis es una enfermedad compleja con gran impacto sobre varias dimensiones de la salud, desde las metabólicas y cardiovasculares hasta las psicológicas, además de su manifestación dermatológica. Aunque se han producido importantes avances en la comprensión de su fisiopatología y en su tratamiento, existen desafíos en relación a la personalización de tratamientos, la accesibilidad a opciones innovadoras y la comprensión completa de los mecanismos que subyacen a la cronicidad de la enfermedad. Si bien nuestra revisión ofrece una perspectiva completa sobre las opciones terapéuticas actuales, la falta de comparaciones entre algunos de los agentes y la heterogeneidad en los diseños de los estudios impiden la generalización de los resultados de algunas de las intervenciones. La principal ventaja radica en la oportunidad de evidenciar la relevancia de los tratamientos dirigidos y su impacto en la calidad de vida de los pacientes.
Es preciso que se realicen mayores inversiones en investigación, no solo en relación a nuevas dianas terapéuticas, sino también en aspectos asociados a la adherencia, el manejo en poblaciones específicas y la comprensión de elementos socioeconómicos que afecten la atención. La vinculación de estudios colaborativos, multicéntricos y longitudinales reviste importancia para cerrar las brechas actuales en el manejo de la enfermedad e impulsar un enfoque más integral y equitativo para abordar la psoriasis en todo el mundo.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
