Introducción
El embarazo ectópico en una cicatriz de cesárea previa (EECC) es la implantación del embrión en el miometrio de una cicatriz generada por un nacimiento por cesárea1. Esta condición tiene una incidencia de 1 por cada 2000 embarazos en mujeres con antecedente de cesárea2. La tasa de cesáreas ha aumentado en las últimas décadas y con ello la incidencia de acretismo placentario. En México, la tasa de nacimientos por cesárea en 2022 fue muy alta, del 53.1%3. La frecuencia de acretismo placentario entre 1930 y 1950 era de 1 por cada 30,000 nacimientos4, y actualmente es de 1 por cada 2625. Este incremento en las tasas de cesáreas y de acretismo placentario, y el desarrollo de mejoras tecnológicas para el diagnóstico prenatal por imagen con ultrasonido y resonancia magnética, han llevado a un aumento de los reportes de casos de EECC1,4. El 52% de estos ocurren con el antecedente de solo una cesárea previa. Esta condición se asocia a altas tasas de morbimortalidad materna, como hemorragia grave, espectro de acretismo placentario y ruptura uterina; por ello, el tratamiento debe indicarse de inmediato una vez que se realiza el diagnóstico1.
No hay consenso sobre la modalidad de tratamiento de estos casos y existen múltiples opciones, que incluyen manejo expectante, manejo médico con metotrexato sistémico o local, manejo quirúrgico conservador por vía histeroscópica o laparoscópica, dilatación y curetaje, embolización de arterias uterinas o histerectomía total. En ocasiones se llegan a combinar distintos abordajes con el fin de mejorar el resultado6.
A continuación, se reporta un caso de EECC que tuvo un resultado exitoso recibiendo manejo conservador con metotrexato sistémico e intrasacular guiado por ultrasonido.
Caso clínico
Paciente de 38 años, gestas 3, cesáreas 2, que acudió al hospital por sangrado transvaginal, con ultrasonido que reportaba saco gestacional de 21 mm, embrión de 6.6 semanas por longitud cráneo-cauda, localizado en la pared anterior del istmo uterino, sugiriendo inserción en cicatriz uterina (Fig. 1). La cuantificación de la subunidad beta de la gonadotropina coriónica humana (hCG-β) se encontraba en 6,402 mUI. Se ofertó tratamiento médico o quirúrgico, explicando los posibles riesgos y complicaciones, y se optó por manejo conservador. Una vez corroborados los valores normales de las pruebas de función hepática se realizó el procedimiento en quirófano, bajo anestesia regional, en posición de litotomía. Se colocó un espejo vaginal y se realizó una punción del saco gestacional transcervical con aguja Echotip de Cook de 22 G y 15 cm, guiada por ultrasonido endovaginal, administrando metotrexato 1 mg/kg intrasacular, y luego una dosis única intravenosa de 50 mg, sin complicaciones. La paciente fue egresada a las 24 horas posterior al procedimiento.
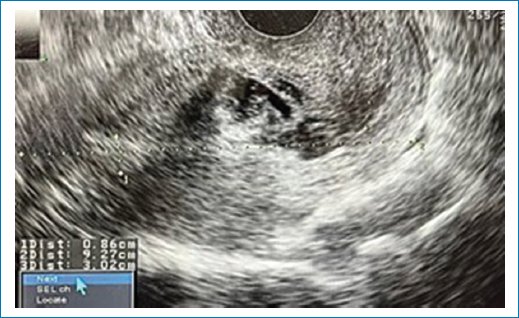
Figura 1. Embarazo en cicatriz uterina de cesárea previa. Embrión de 6.6 semanas por longitud cráneo-cauda.
En la primera semana después del procedimiento la hCG-β se encontraba en 2,807 mUI, y a las 3 semanas en 63 mUI. Ultrasonográficamente se observó un saco gestacional de 11 mm y ausencia de embriocardio (Fig. 2). A las 6 semanas se obtuvo negativización de la hormona, con un saco gestacional por ultrasonido apenas visible de 6 × 4 mm. Al tercer mes, la paciente presentó metrorragia correspondiente al ciclo menstrual.
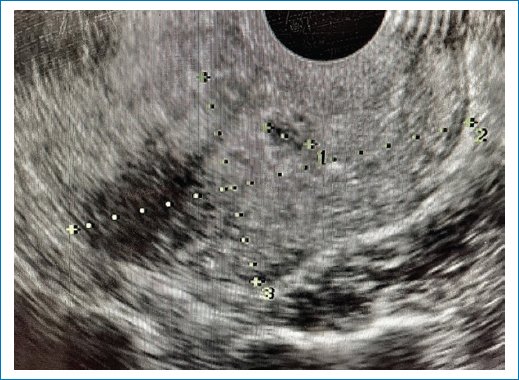
Figura 2. Ultrasonido a las 3 semanas.
Discusión
La patogénesis del EECC involucra la implantación del blastocisto dentro de dehiscencias microscópicas en el tracto de una cicatriz de cesárea previa. Por esta razón, el EECC y el acretismo placentario parecen compartir una misma vía fisiopatológica, pudiendo existir ambas como parte del desarrollo de una enfermedad en común1.
El EECC tiene dos patrones de implantación, los cuales adopta la Society for Maternal-Fetal Medicine (SMFM) en su última revisión y que al parecer tienen implicaciones pronósticas:
- – Tipo 1 o endógeno (sobre la cicatriz): el crecimiento se da hacia la cavidad endometrial, presentándose posteriormente con características clínicas y hallazgos sonográficos de acretismo placentario.
- − Tipo 2 o exógeno (dentro de la cicatriz): hay una implantación más profunda, penetrando la pared uterina anterior, invadiendo la vejiga y pudiendo provocar ruptura uterina1,7,8.
Un consenso de expertos en China estableció en el año 2016 una clasificación con tres tipos, que ha demostrado proveer una mejor orientación para el tratamiento:
- – El tipo I es endógeno, y el crecimiento es hacia el espacio ístmico-cervical, con un grosor miometrial entre el saco y la vejiga > 3 mm.
- − El tipo II también es endógeno, pero con un grosor miometrial ≤ 3 mm.
- − El tipo III es exógeno, con crecimiento hacia la vejiga y la cavidad abdominal.
Suxia et al.9 reportaron una serie de 725 casos, de los cuales 162 (22.4%) fueron de tipo I, 465 (64.1%) de tipo II y 98 (13.5%) de tipo III.
El tratamiento se basa en el tipo de implantación, la edad gestacional, el deseo de fertilidad, la gravedad de los síntomas y el estado hemodinámico10. Se puede preservar el útero hasta en el 95% de los casos11. La administración de 1 mg/kg de metotrexato, sistémico o local guiado por ultrasonido, o la combinación de ambos, se ha utilizado cuando la paciente se encuentra hemodinámicamente estable y con deseos de fertilidad12. La administración sistémica sola ha demostrado una tasa de fallo de hasta el 50%13, posiblemente debido a la pobre absorción del medicamento a través del tejido cicatricial fibroso10. Por esta razón, se ha propuesto la inyección dentro del saco gestacional como una opción más efectiva al poder administrar una dosis más alta sin los efectos adversos de la administración sistémica14.
En una serie de 54 pacientes tratadas con metotrexato local, ninguna requirió tratamiento quirúrgico complementario y el 76% de ellas lograron un embarazo posterior15. En otra serie de 30 pacientes que recibieron el mismo tratamiento local, cinco presentaron falla al tratamiento16. Al comparar con las pacientes que tuvieron un tratamiento exitoso, las dos variables que mostraron significancia estadística fueron el tipo de implantación, siendo más común el tipo exógeno en el grupo con falla al tratamiento (80% vs. 24%), y los niveles de hCG-β, con una media mayor en el grupo fallido (81,418 vs. 28,484 mUI/ml)16. En una revisión de casos realizada por Cheung17, de 96 pacientes con EECC el 73.9% tuvieron un resultado exitoso con metotrexato local, y el porcentaje aumentó al 88.5% posterior a una dosis adicional local o sistémica. Un nivel de hCG-β > 100,000 mUI fue la única variable que se asoció a falla al tratamiento. La dosis de metotrexato local utilizada en la mayoría de los casos fue de 1 mg/kg, con una dosis máxima de 50 mg17. En el estudio de Suxia et al.9 con 725 pacientes, seis pacientes con tipo III fueron tratadas con metotrexato sistémico, sin éxito. No hubo pacientes tratadas con metotrexato local. Estos casos recibieron tratamiento quirúrgico combinado con laparoscopia y curetaje guiado por histeroscopia, o curetaje posterior a embolización de arterias uterinas, con tasas de éxito del 96.6% y el 87.9%, respectivamente9.
El cloruro de potasio local también se ha utilizado de manera exitosa, especialmente en los casos de EECC heterotópicos con feto intrauterino viable, con el objetivo de evitar el efecto teratogénico del metotrexato18,19.
Es importante tener en cuenta que los niveles de hCG-β, el volumen del saco gestacional y la vascularidad pueden aumentar transitoriamente al administrar metotrexato, debido a la inflamación generada por la necrosis de las células trofoblásticas y la liberación de la hCG almacenada. Se debe hacer un seguimiento seriado de la hCG-β, ya que puede tomar varias semanas hasta su negativización, con una media de 88 días (rango: 26-177)20, lo cual concuerda con nuestro caso, en el que la hormona negativizó a los 42 días.
Aunque la SMFM no recomienda el manejo expectante1, diversos estudios han evaluado los resultados en pacientes que decidieron continuar con el embarazo y los factores de riesgo asociados a complicaciones. Los hallazgos que se asocian a buen pronóstico son EECC de tipo I, mayor grosor miometrial y signo de crossover (COS) tipo 221. En un estudio se determinó que un grosor miometrial > 3.3 mm entre el saco gestacional y la vejiga tiene una sensibilidad del 80% y una especificidad del 81% para descartar una complicación grave22. El COS se determina con una imagen del útero en sagital, trazando una línea longitudinal a través del endometrio que conecta el orificio cervical interno con el fondo uterino. En el COS1, al menos dos tercios del saco gestacional se encuentran por arriba de la línea endometrial, y en el COS2, menos de dos tercios del saco gestacional se encuentran por arriba de la línea endometrial. La proporción de placenta percreta fue mayor en COS1 que en COS2 (83% vs. 42%)23.
En una revisión de 44 casos de EECC que recibieron manejo expectante, en 32 (73%) se logró un recién nacido vivo, con 9 (20%) de ellos que nacieron antes de las 34 semanas. Sin embargo, el 70% requirieron histerectomía por acretismo placentario como principal indicación24. En otro estudio, los casos con implantación endógena tuvieron una tasa de histerectomía del 17%, en comparación con el 91% en el grupo de implantación exógena. El grosor miometrial en el primer trimestre tuvo diferencias significativas entre las pacientes que requirieron histerectomía y aquellas que no la requirieron, con una media de 1 mm y 5 mm, respectivamente25.
Conclusión
El uso de metotrexato sistémico y local combinado es una opción segura y tiene una alta tasa de efectividad en el tratamiento del EECC. Es importante hacer una adecuada evaluación de las pacientes, considerando la edad gestacional, el tipo de implantación, los niveles de hCG-β y el grosor miometrial, para decidir el mejor tratamiento.
Agradecimientos
Los autores agradecen al Hospital de la Mujer Puebla por la gran afluencia de pacientes que posee, al ser el centro de referencia del Estado, lo que permite atender gran cantidad de casos diariamente. Asimismo, agradecen al Dr. A. Castilla-Zenteno por sus enseñanzas, por transmitir sus conocimientos y por la gran destreza que desempeña como obstetra y perinatólogo.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki. Los procedimientos fueron autorizados por el Comité de Ética de la institución.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han seguido los protocolos de confidencialidad de su institución, han obtenido el consentimiento informado de la paciente, y cuentan con la aprobación del Comité de Ética. Se han seguido las recomendaciones de las guías SAGER, según la naturaleza del estudio.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.